- »ż·Ö
- 151
- ×¢²įŹ±¼ä
- 2015-4-21
- »ż·Ö
- 151
 
|
ChemBio 3DŹĒŅ»æī×ØŅµµÄČżĪ¬·Ö×Ó½į¹¹ŃŻŹ¾Čķ¼ž£¬ĖüÓėChemDraw²»Ķ¬£¬ChemBio 3DÄÜĶعż3D½ØÄ£”¢æÉŹÓ»ÆŗĶ¼ĘĖćµČ·įø»¹¦ÄÜ£¬Äܹ»°ļÖś“ó¼ŅøüŗĆ”¢øüæģµŲČ·¶Ø³öŃŠ¾æÖŲµć£¬“Ó¶ųĢįøßÉś²śĮ¦£¬æģĖŁ“ļ³ÉŃŠ¾æÄæ±ź”£¶ų·Ö×Ó¹ģµĄĄķĀŪÖŠµÄ×īøßÕ¼ÓŠ£ØHOMO£©ŗĶ×īµĶæÕ¹ģµĄ£ØLUMO£©ŌŚ·Ö×Ó·“Ó¦ÖŠÓŠ×ÅÖŲ“óŅāŅ壬±ŹÕß¾ĶŅŌŗ¬ÓŠĖ«¼üµÄ×ī¼ņµ„·Ö×ÓŅŅĻ©Ą“²āŹŌĖ«¼üµÄ·“Ó¦»īŠŌ”£
1. ½ØĮ¢Ä£ŠĶ
£Ø1£©“ÓFile²Ėµ„ÖŠ£¬Ń”ŌńNew Model”£
£Ø2£©ŌŚæņÖŠŹäČėCH2CH2£¬²¢µ„»÷Enter¼ü”£“ĖŹ±£¬Ņ»øöŅŅĻ©·Ö×Ó±»½ØĮ¢”£
2. ³É¼ü¹ģµĄ
£Ø1£©“ÓAnalyze²Ėµ„ÖŠ£¬Ń”ŌńExtended Huckel Surfaces”£
£Ø2£©“ÓView²Ėµ„µÄ×Ó²Ėµ„Molecular SurfacesÖŠ£¬Ń”ŌńMolecular Orbitals”£
£Ø3£©ŌŚ¹ģµĄĮŠ±ķæņÖŠ£¬Ń”ŌńHOMO£ØN=6£©”£
£Ø4£©µ„»÷Show Surface°“Å„”£
“ĖŹ±Ņ»øöÖŲµž¼üµÄÄ£ŠĶ³öĻÖ£¬ŹĒp³É¼ü¹ģµĄ£¬ČēĻĀĶ¼
p³É¼ü¹ģµĄ
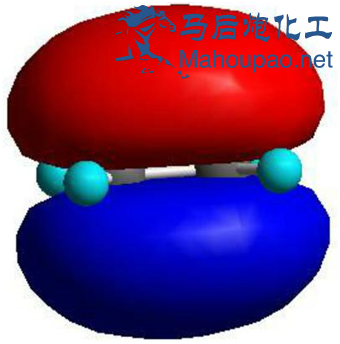
p³É¼ü¹ģµĄ
3. ·“¼ü¹ģµĄ
£Ø1£©ŌŚ¹ģµĄĮŠ±ķæņÖŠ£¬Ń”ŌńLUMO£ØN=7£©”£
£Ø2£©µ„»÷Show Surface°“Å„”£
“ĖŹ±Ņ»øöÅųā¼üµÄÄ£ŠĶ³öĻÖ£¬ŹĒp·“¼ü¹ģµĄ£¬ČēĻĀĶ¼”£
p·“¼ü¹ģµĄ
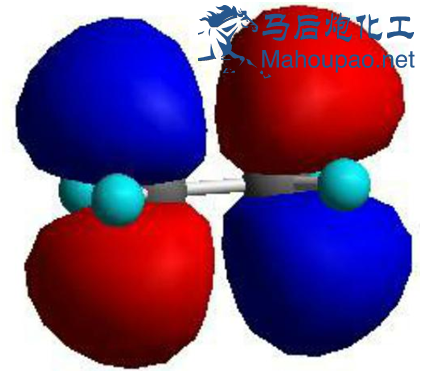
p·“¼ü¹ģµĄ
”¾ĖµĆ÷”æ12øö²»Ķ¬¹ģµĄÖŠÖ»ÓŠ2øö¹ģµĄŹĒ¶ŌĖ«¼üÓŠ¹±Ļ׵ģ¬ĘäÓą10øö“ś±ķs¹ģµĄµÄ²»Ķ¬×÷ÓĆ”£Ö»ÓŠp¹ģµĄ±»Éę¼°ŌŚHOMOŗĶLUMOÖŠ”£ÓÉÓŚHOMO ŗĶLUMOæŲÖĘ·Ö×ӵķ“Ó¦»īŠŌ£¬Ņņ¶ųŅ²æÉŅŌĖµŅŅĻ©p¹ģµĄŠĪ³ÉµÄ¼üæŲÖĘĖüµÄ·“Ó¦»īŠŌ”£ÕāŅ²ŹĒŅ»øöĢŲŹāµÄ¹ęĀÉ£ŗp¹ģµĄŠĪ³ÉµÄ¼ü±Čs¹ģµĄŠĪ³ÉµÄ¼ü»īŠŌŅŖ“ó”£
ĶعżĪÄÖŠŅŅĻ©µÄ°øĄż£¬Ļ£Ķū“ó¼ŅæÉŅŌŹģĻ¤×īøßÕ¼ÓŠ£ØHOMO£©ŗĶ×īµĶæÕ¹ģµĄ£ØLUMO£©µÄĄķĀŪ£¬Čē¹ū“ó¼Ņ»¹ĻėĮĖ½āøü¶ąChemDraw½Ģ³Ģ·½ĆęµÄÄŚČŻ£¬»¶Ó“ó¼ŅĒ°ĶłChemDrawÖŠĪĹŁĶųĮĖ½āøü¶ąÄŚČŻ£”
øü¶ąÄŚČŻ£ŗChemDraw** |
|
 ·¢±ķÓŚ 2015-5-25 16:27:31
ĻŌŹ¾Č«²æĀ„²ć
·¢±ķÓŚ 2015-5-25 16:27:31
ĻŌŹ¾Č«²æĀ„²ć